Cell Death and Differentiation|戈万忠课题组与吕卫国课题组合作揭示R-loops稳态调控分子机制
R-Loops主要指转录过程中在基因组上形成的三条核苷酸链的特殊结构,其包含转录时新生RNA链与DNA模板链形成的RNA:DNA杂交链以及非模板DNA单链。R-Loops广泛存在于多种生物体中,并在多种生物学过程中发挥调控作用,例如DNA复制、基因表达、免疫球蛋白类别转换重组、DNA甲基化及组蛋白修饰和DNA损伤修复。虽然许多自然产生的R-loops在正常生理学过程是有益的,但是细胞中异常R-loops的积累通常会通过阻止DNA复制叉的延伸和促进DNA双链断裂引起DNA损伤和基因组不稳定性。已有研究发现包括肿瘤和神经障碍等多种人类疾病中都存在异常R-loops的积累,但是其致病机理并不完全清楚。因此,解析细胞内R-loops水平及其分布的分子调控机制具有十分重要的意义。NKAP编码一个高度保守的核质蛋白,并定位于核斑,在RNA剪接和加工过程中发挥作用。早期研究发现NKAP在T细胞发育成熟及造血干细胞的维持和存活过程中起着重要作用。有研究表明NKAP错义突变是造成马凡样特征和智商障碍的一种神经发育疾病的原因。此外,NKAP也参与细胞有丝分裂染色体排列的调控和染色体稳定性的维持,并且其在多种肿瘤中表达异常或者发生突变。因此,NKAP在细胞中可能通过多种不同的分子机制发挥其功能。
团队研究人员在探究NKAP是否通过有丝分裂调控以外机制来影响基因组不稳定性和肿瘤发生的实验过程中,意外发现其在R-loops稳态维持和阻止DNA损伤中的重要功能。研究人员首先在模式细胞U2OS中敲降NKAP的表达,结果发现细胞中DNA损伤的两个经典标记物 γ-H2AX 和 53BP1表达大量升高,结合彗星实验证实NKAP敲降会导致细胞中DNA单双链的断裂,同时微核与染色体桥结构在NKAP敲降细胞中也增加,这些结果表明NKAP敲降会造成DNA损伤和基因组不稳定(图1)。
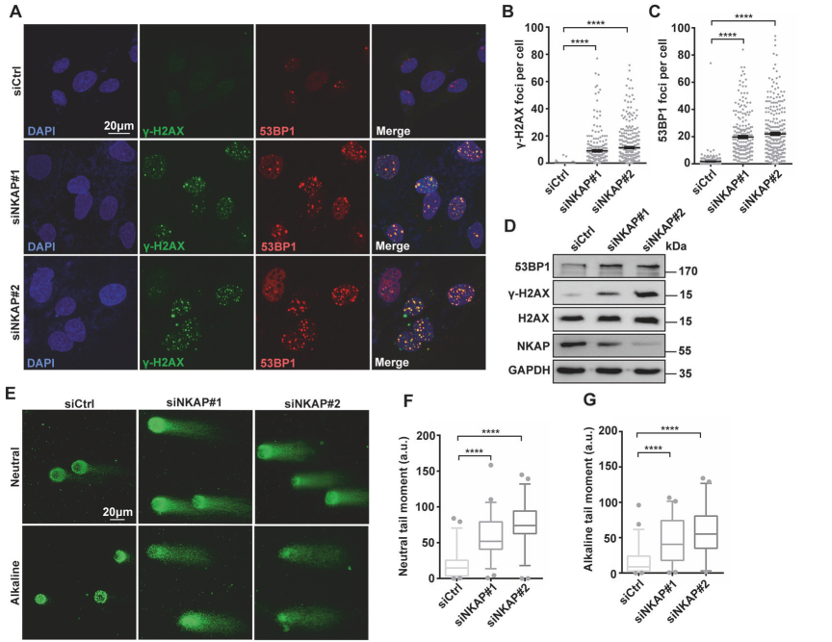
图1. 敲低NKAP导致DNA损伤和基因组不稳定性
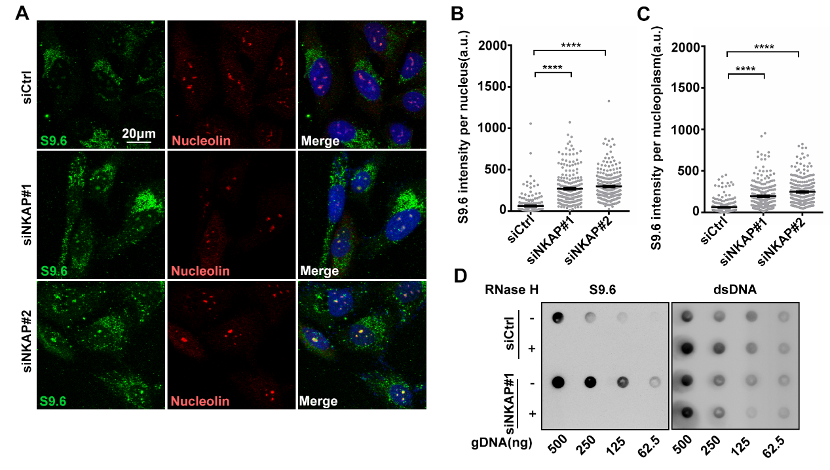
图2. 敲低NKAP造成细胞核内R-Loops积累
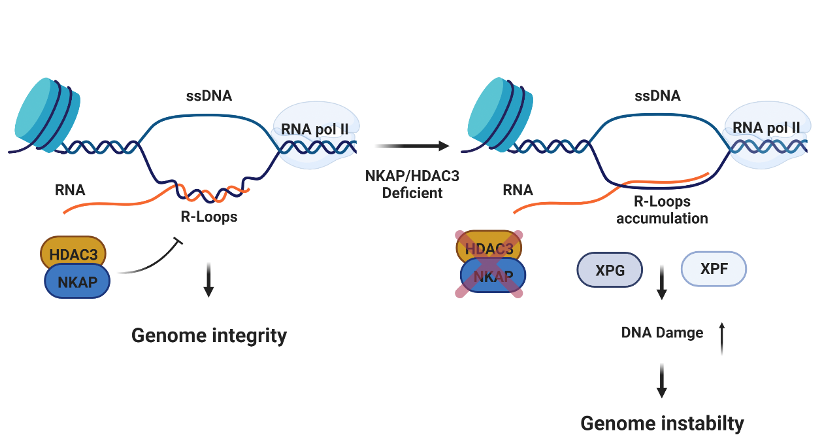
综合以上实验结果,该研究不仅揭示了NKAP和HDAC3在R-loops稳态维持中的功能,而且提出了NKAP/HDAC3复合物阻止R-loops及DNA复制压力形成的模型,为利用R-loops调控因子来开发抗肿瘤药物提供了思路(图3)。
















 地址:浙江省杭州市上城区凯旋街道268号浙江大学医学院华家池校区
地址:浙江省杭州市上城区凯旋街道268号浙江大学医学院华家池校区 电话/传真: 0571-87061501/0571-87061878
电话/传真: 0571-87061501/0571-87061878 邮编:310029
邮编:310029 邮箱:qinjiale@zju.edu.cn
邮箱:qinjiale@zju.edu.cn